Задача 5.1. Определите объем (н.у.) кислорода, необходимый для сжигания 1 кг бутана.
Решение. Находим количество вещества бутана С4Н10, если М(С4Н10) = 58 г/моль:
v = m/М = 1000 г / (58 г/моль) = 17,24 моль.
Записываем уравнение реакции:
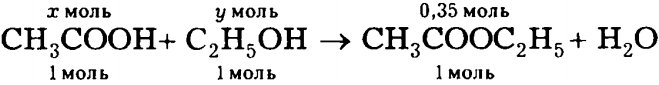
По уравнению реакции находим количество вещества кислорода:
х = v(O2) = 17,24 • 13/2 = 112,1 моль.
Находим объем кислорода:
v(O2) = v • VM = 112,1 • 22,4 = 2510 л = 2,51 м3.
Задача 5.2. Определите массу уксусной кислоты и массу этанола, которые необходимы для получения 30,8 г этилацетата.
Решение. Зная молярную массу этилацетата М(СН3СООС2Н5) = 88 г/моль, определим количество вещества этилацетата
v(C2H5COOCH3) = m/M = 30,8 г / (88 г/моль) = 0,35 моль. Напишем уравнение реакции этерификации:
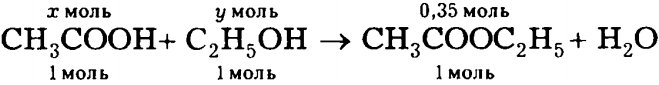
Из уравнения видно, что
v(СН3СООН) = v(СН3ОН) = v(СН3СООС2Н5) = 0,35 моль.
Зная
М(СН3СООН) = 60 г/моль
и
М(С2Н5ОН) = 46 г/моль,
находим:
m(СН3СООН) = v • М = 0,35 моль • 60 г/моль = 21,0 г
и
m(С2Н5ОН) = v • М = 0,35 моль • 46 г/моль = 16,1 г.
[]